 |
 |
AbstractBackground and ObjectivesClaudin-1 (CLDN-1) is the major component of tight junctions and functions in controlling cell to cell adhesion. Certain claudins were expressed aberrantly and proved to have prognostic significance in various human cancers. However, its clinical significance has been poorly understood in head and neck squamous cell carcinoma (HNSCC). The aim of this study was to investigate the relationship between CLDN-1 expression and clinicopathologic parameters in HNSCC.
Subjects and MethodThe surgical specimens of primary HNSCCs from a consecutive cohort of 91 patients were retrospectively collected. Immunohistochemical staining for CLDN-1 was performed blindly by two pathologists. CLDN-1 staining intensity was scored semi-quantitatively on a scale of 0 to 3 (0: negative; 1: weak; 2: moderate; 3: strong). For the statistical analysis, the expression levels were classified as low (negative and weak) and high (moderate and strong). Next, the association between CLDN-1 expression and clinicopathological features & clinical outcomes was analyzed.
ResultsThe increased CLDN-1 expression was significantly associated with lymphatic invasion (p=0.019). The expression level of CLDN-1 was not associated with pathological T stage, lymph node metastasis or recurrence. Kaplan-Meier analysis found that 3-year overall survival (OS) rate was 53% in patients with high level CLDN-1 expression and 74% in patients with low level CLDN-1 expression. It also found that 5-year OS rate was 49% in patients with high level CLDN-1 expression and 68% in patients with low level CLDN-1 expression. A significantly poor OS rate was recorded in patients with high level of CLDN-1 expression compared to patients with low level CLDN-1 expression (p=0.022).
ÏÑú ΰÝÎëêÍ≤ΩÎ∂Ä Ìé∏ÌèâÏÑ∏Ìè¨Ïïî(head and neck squamous cell carcinoma, HNSCC)ÏùÄ ÏÝÑ ÏÑ∏Í≥ÑÏóêÏÑú ÎߧÎÖÑ 650000ͱ¥Ïù¥ ÏÉàΰú ÏßÑÎã®ÎêòÍ≥Ý, Ïó∞Í∞Ñ 350000ͱ¥Ïùò ÏǨÎßùΕÝÏùÑ Í∏∞ΰùÌïòÎäî Ïó¨ÏÑØ Î≤àÏß∏ΰú ÌùîÌïú ÏïîÏù¥Îã§[1]. ÎëêÍ≤ΩÎ∂ÄÏïîÏùò Î∂ÑÏûêÏÝÅ Í∏∞ÏÝÑÏùÄ ÏïîÏùò Í∑ºÎ≥∏ÏÝÅÏù∏ Î≥ëÏù∏ÏùÑ Ïûò Ïù¥Ìï¥ÌïòÍ≥Ý ÌôòÏûêÏùò ÏòàÌõÑÏôÄ ÏπòΣå Í≤∞Í≥ºÎ•º Ìñ•ÏÉÅÏãúÌǧÍ∏∞ ÏúÑÌï¥ Íæ∏ϧÄÌûà Ïó∞͵¨ÎêòÏñ¥ÏôîÏúºÎÇò ÏßÄÏÜçÏÝÅÏù∏ Ïó∞͵¨ÏóêÎèÑ Î∂à͵¨ÌïòÍ≥Ý ÎëêÍ≤ΩÎ∂ÄÏïî ÌôòÏûêÏùò ÏǨÎßùΕÝÏùÄ ÌŨÍ≤å Í∞êÏÜåÌïòÏßÄ ÏïäÏïòÎã§[2]. Îî∞ÎùºÏÑú ÏïûÏúºÎ°úÎäî Í∏∞Ï°¥Ïóê Ïûò ÏïåÎݧÏßÑ ÏòàÌõÑ Ïù∏ÏûêÏóêÏÑú Îçî ÎÇòÏïÑÍ∞Ä ÏÉàΰúÏö¥ ÏòàÌõÑ Ïù∏ÏûêÎì§Ïóê ÎåÄÌïú Ïó∞͵¨Í∞Ä ÌïÑÏöîÌïú Ïã§ÏÝïÏù¥Îã§. ϵúÍ∑º ÏïîÏùò ÏѱÏû• Î∞è ÏÝÑÏù¥Ïóê ÎåÄÌïú Ïó∞͵¨Í∞Ä Ïù¥Î£®Ïñ¥ÏßÄΩ¥ÏÑú Î∂ÄÏ∞© Î∂ÑÏûê(adhesion molecule)Ïóê Í¥ÄÌïú Í¥ÄÏã¨Ïù¥ ÎÜíÏïÑÏ°åÍ≥Ý, Ïó¨Îü¨ Ïó∞͵¨ÏóêÏÑú Î∂ÄÏ∞© Î∂ÑÏûêÎì§Ïù¥ ÏïîÏùò ÏßÑÌñâÏóê ÏûàÏñ¥ ϧëÏöîÌïú Ïó≠ÌïÝÏùÑ ÌïúÎã§Í≥Ý Î≥¥Í≥ÝÎêòÍ≥Ý ÏûàÎã§[3,4].
ClaudinÏùÄ ÏÑ∏Ìè¨ Í∞Ñ Î∂ÄÏ∞© Í∏∞Îä•ÏùÑ Îã¥ÎãπÌïòÎäî Ïó∞Í≤∞Î≥µÌï©Ï≤¥(junctional complex) ϧë Î∞ÄÏ∞©Ïó∞ÏÝë(tight junction)ÏùÑ Ïù¥Î£®Îäî Ï£ºÏöîÌïú ÎßâÎã®Î∞±Ïßà(transmembrane protein)Ïù¥Îã§. Î∞ÄÏ∞©Ïó∞ÏÝëÏùÄΨº, Ïù¥Ïò®, Îã®Î∞±Ïßà Î∂ÑÏûêÏôÄ Í∞ôÏùÄ Î¨ºÏßàÏù¥ ÏÑ∏Ìè¨ÏôÄ ÏÑ∏Ìè¨ ÏǨÏù¥ Í≥µÍ∞Ñ(paracellular pathway)ÏùÑ ÌܵÌï¥ Ïù¥ÎèôÌïòÎäî Í≤ÉÏùÑ ÎßâÎäî Ïû•Î≤Ω(barrier) Ïó≠ÌïÝÏùÑ ÌïòΩ∞, ÎèôÏãúÏóê ÏÑ∏Ìè¨ÎßâÏùÑ ÏÝïÎã®Î∂Ä(apical)ÏôÄ Í∏∞ÏÝÄÏ∏°Î∂Ä(basolateral) ÏòÅÏó≠ÏúºÎ°ú ÎÇòÎàÑÏñ¥ ÏÑ∏Ìè¨Ïùò Í∑πÏѱ(cell polarity)ÏùÑ ÎùÑÍ≤å ÌïúÎã§[5]. ClaudinÏùÄ ÌòÑÏû¨ÍπåÏßÄ 24Í∞úÏùò ÏïÑÌòïÏù¥ Î∞ùÌòÄÏ°åÏúºÎ©∞, Ï°∞ÏßÅÎßàÎ㧠Í∞ÅÍ∞Å Îã§Î•∏ ÏïÑÌòïÏù¥ Î∞úÌòÑÎêúÎã§[2]. Ïó¨Îü¨ ÏïîÏóêÏÑú claudinÏùò Î∞úÌòÑÏóê ÎåÄÌïú Ïó∞͵¨Îì§Ïù¥ Î≥¥Í≥ÝÎêòÍ≥Ý ÏûàÏúºÎ©∞, Ï°∞ÏßÅ Î∞è Î≥ëÎ≥ÄÏóê Îî∞Îùº Î∞úÌòÑÎêòÎäî claudinÏùò Ï¢ÖΕòÏôÄ Î∞úÌòÑ ÏñëÏÉÅÏù¥ Îã¨Îùº claudinÏùÄ Ï°∞ÏßÅ ÌäπÏù¥ÏÝÅ Í∏∞Îä•ÏùÑ Í∞ÄÏßà Ïàò ÏûàÎã§[2,6].
ÎëêÍ≤ΩÎ∂ÄÏïîÏóêÏÑúÎäî claudin-1(CLDN-1)Ïù¥ claudinÏùò 24Í∞ú ÏïÑÌòï ϧëÏóêÏÑú Í∞ÄÏû• ÌôúÎ∞úÌïòÍ≤å Ïó∞͵¨ÎêòÍ≥Ý ÏûàÏúºÎ©∞, ÎëêÍ≤ΩÎ∂Ä Ìé∏ÌèâÏÑ∏Ìè¨Ïïî ÏïàÏóêÏÑúÎäî Ï£ºÎ°ú ͵¨Í∞ïÏïîÍ≥º CLDN-1Ïóê ÎåÄÌïú Ïó∞͵¨Í∞Ä Î≥¥Í≥ÝÎêòÏóàÎã§[2,7]. Í∑∏Îü¨ÎÇò ͵¨Í∞ïÏïî Ïô∏ Îã§Î•∏ ÎëêÍ≤ΩÎ∂ÄÏïîÏóêÏÑú CLDN-1Ïùò Î∞úÌòÑ ÏñëÏÉÅÍ≥º ÏûÑÏÉÅ Î≥ëζ¨ÌïôÏÝÅ Ïó∞Í¥ÄÏѱÏóê ÎåÄÌï¥ÏÑúÎäî ÏïÑÏßÅ Ï∂©Î∂ÑÌïú Ïó∞͵¨Í∞Ä Ïù¥Î§ÑÏßÄÏßÄ ÏïäÏïòÎã§. Ïù¥Ïóê Î≥∏ Ïó∞͵¨ÏûêÎì§ÏùÄ Íµ¨Í∞ïÏïîÏùÑ ÎπÑΰØÌïòÏó¨ Ïó¨Îü¨ ÎëêÍ≤ΩÎ∂ÄÏïî ÌôòÏûêΕº ÎåÄÏÉÅÏúºÎ°ú CLDN-1Ïùò Î∞úÌòÑ ÏñëÏÉÅ Î∞è Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ÏûÑÏÉÅÎ≥ëζ¨ÌïôÏÝÅ ÌäπÏѱÏùÑ ÏïåÏïÑÎ≥¥Í≥ÝÏûê Î≥∏ Ïó∞͵¨Î•º ÏßÑÌñâÌïòÏòÄÎã§.
ÎåÄÏÉÅ Î∞è Î∞©Î≤ïÎåÄ ÏÉÅ2006ÎÖÑ 1Ïõî~2015ÎÖÑ 6ÏõîÍπåÏßÄ ÎëêÍ≤ΩÎ∂Ä Ìé∏ÌèâÏÑ∏Ìè¨Ïïî(HNSCC)ÏùÑ ÏßÑÎã®Î∞õÍ≥Ý ÏàòÏàÝÏÝÅ ÏπòΣåΕº ÏãúÌñâÌïú 91ΙÖÏùÑ Ïó∞ÏÜçÏÝÅ ÏΩîÌò∏Ìä∏ Î∞©Ïãù(consecutive cohort study)ÏúºÎ°ú ÏÑÝÏÝïÌïòÏòÄÎã§. Î≥ëÎ≥ÄÏùò ÏõêÎ∞ú Î∂ÄÏúÑÎäî ͵¨Í∞ï 23Ïòà, ͵¨Ïù∏Îëê 15Ïòà, ÌõÑÎëê 33Ïòà, ÌïòÏù∏Îëê 13Ïòà, ÎπÑÎ∂ÄÎπÑÎèô 7ÏòàÏòÄÍ≥Ý, ÏàòÏàÝ Ïãú ÏÝÅÏ∂úÎêú ÏõêÎ∞ú Î∂ÄÏúÑ Ï¢ÖÏñëÏùÑ ÎåÄÏÉÅÏúºÎ°ú CLDN-1Ïóê ÎåÄÌïú Ω¥Ïó≠Ï°∞ÏßÅ ÌôîÌïôÏóºÏÉâÏùÑ ÏãúÌñâÌïòÏòÄÎã§. Ïó∞͵¨ ÎåÄÏÉÅÏùò Î≥ëζ¨ ÏßÑÎã® Î≥¥Í≥ÝÏÑúΕº Ï∞∏Í≥ÝÌïòÍ≥Ý Î≥¥Í¥ÄÎêú Ï°∞ÏßÅ Ïä¨ÎùºÏù¥ÎìúΕº Ïû¨Í≤ÄÌÜÝÌïòÏó¨ Ï°∞ÏßÅÌïôÏÝÅ ÏúÝÌòïÍ≥º Ïπ®Ïäµ ÍπäÏù¥, Î∂ÑÌôîÎèÑ, ζºÌîÑÏÝà ÏÝÑÏù¥ ÏúÝΨ¥Î•º Ï°∞ÏǨÌïòÏòÄÍ≥Ý, ÎåÄÏÉÅ ÌôòÏûêÏùò ÏùòΨ¥Í∏∞ΰùÍ≥º Ï∂îÏÝÅ Ï°∞ÏǨΕº ÌܵÌï¥ ÎÇòÏù¥, ÏѱÎ≥Ñ Îì±Ïùò ÏûÑÏÉÅÏñëÏÉÅÍ≥º TNM Î≥ëÍ∏∞, ÏûÑÏÉÅÎ≥ëÍ∏∞ Î∞è ÏÉùÏ°¥ ÏúÝΨ¥Î•º Ï°∞ÏǨÌïòÏòÄÎã§. 91ΙÖÏùò ÌôòÏûêÏóêÏÑú Í≤ΩÎ∂ÄÏÝàÏÝúÏàÝÏùò ÏãúÌñâ Ïó¨Î∂ÄÎäî ÏàòÏàÝ ÏÝÑ ÏòÅÏÉÅÌïôÏÝÅ Í≤ÄÏǨ Í≤∞Í≥ºÏôÄ ÏõêÎ∞ú Î∂ÄÏúÑ Îì± ÏûÑÏÉÅ ÏñëÏÉÅÏùÑ Í≥ÝÎݧÌïòÏó¨ Í≤∞ÏÝïÌïòÏòÄÎã§. Ï∂îÏÝŠͥÄÏ∞∞ÏùÄ ÏàòÏàÝ ÌõÑ Ï≤´Ìï¥ÏóêÎäî 1~3Í∞úÏõîÎßàÎã§, Îëê Î≤àÏß∏ÏôÄ ÏÑ∏ Î≤àÏß∏ Ìï¥Ïóê 2~4Í∞úÏõîÎßàÎã§, Îѧ Î≤àÏß∏, Îã§ÏÑØ Î≤àÏß∏ Ìï¥ÏóêÎäî 3~6Í∞úÏõîÎßàÎã§, Í∑∏ Ïù¥ÌõÑΰúÎäî ÌôòÏûêÏùò ÏÉÅÌÉú Î∞è ϶ùÏÉÅÏóê Îî∞Îùº 6Í∞úÏõî~1ÎÖÑÎßàÎ㧠Ïô∏ÎûòΕº Î∞©Î¨∏ÌïòÎèÑΰù ÌïòÏòÄÍ≥Ý, Ω¥Î∞ÄÌïú Ïù¥ÌïôÏÝÅ Í≤ÄÏǨ Î∞è ÎÇ¥ÏãúÍ≤Ω Í≤ÄÏǨÏôÄ ÏÝïÍ∏∞ÏÝÅÏù∏ ÏòÅÏÉÅÌïôÏÝÅ Í≤ÄÏǨΕº ÌܵÌï¥ Ïû¨Î∞ú Ïó¨Î∂ÄΕº ÌèâÍ∞ÄÌïòÏòÄÎã§. ÏÝÑÏ≤¥ ÏÉùÏ°¥ Í∏∞Í∞ÑÏùÄ ÏπòΣå ÏãúÏûëÏùºÎ∂ÄÌÑ∞ ÏǨÎßùÎ≥¥Í≥ÝÏùº ÎòêÎäî ÎßàÏßÄÎßâ Ï∂îÏÝÅÏùºÍπåÏßÄΰú ÏÇ∞ÏÝïÌïòÏòÄÎã§. ÌôòÏûêÍ∞Ä ÏǨÎßù Ïãú ÏǨÎßù ÏõêÏù∏ÏùÑ Î∂ÑÏÑùÌïòÏó¨ ÎëêÍ≤ΩÎ∂ÄÏïîÏúºÎ°ú ÏǨÎßùÌïú ÌôòÏûêÎì§ÏùÑ ÎåÄÏÉÅÏúºÎ°ú ÏßàÎ≥ë ÌäπÏù¥ ÏÉùÏ°¥Ïú®(disease specific survival)ÏùÑ Íµ¨ÌïòÏòÄÍ≥Ý, ÎëêÍ≤ΩÎ∂ÄÏïîÏù¥ ÏǨÏù∏Ïù¥ Îêú Í≤ΩÏö∞ÎßåÏùÑ Í≥ÝÎݧÌïú ÏÉùÏ°¥Ïú®Î°ú ÏÝïÏùòÌïòÏòÄÎã§.
Î∞© Î≤ïΩ¥Ïó≠Ï°∞ÏßÅÌôîÌïôÏóºÏÉâÌè¨Î•¥Îßêζ∞Ïóê Í≥ÝÏÝïÎêú Ï°∞ÏßÅÏùÑ ÏÝêÏßÑÏÝÅ Í≥ÝÎÜçÎèÑÏùò ÏóêÌÉÑÏò¨Î°ú ÌÉàÏàòÏãúÌǧÍ≥Ý ÌååÎùºÌïÄÏóê Ìè¨ÎߧÏãúϺ∞Îã§. ÌååÎùºÌïÄ Î∏îΰùÏùÑ Ìëú준 ÌöåÏÝÑÌòï Î∞ïÏÝàÍ∏∞(rotatory microtome)Εº ÏǨÏö©ÌïòÏó¨ 4 Œºm Îëêͪòΰú ÏÝàÎã®ÌïòÍ≥Ý, ÏàòÎèÑÏàòΰú ÏÑ∏ÏÝï ÌõÑ ÏÉà Ïä¨ÎùºÏù¥ÎìúÏóê ÏòÆÍ≤ºÎã§. BOND polymer intense detection system(Vision BioSystems, Mount Waverley, Australia)ÏùÑ ÏÝúÏ°∞ÏǨÏùò ÏßÄÏπ®Ïóê Îî∞Îùº ÏǨÏö©ÌïòÏó¨ Ï°∞ÏßÅÏùÑ Î©¥Ïó≠Ï°∞ÏßÅÌôîÌïôÏóºÏÉâ Ìï®ÏúºÎ°úÏç® CLDN-1 Îã®Î∞±Ïùò Î∞úÌòÑÏùÑ ÌèâÍ∞ÄÌïòÏòÄÎã§. Ï°∞ÏßÅ ÏÝàÌé∏ÏùÑ Bond dewax Ïö©Ïï°(Vision BioSystems)ÏúºÎ°ú ÌÉàÌååÎùºÌïÄÌôî(deparaffinization)ÌïòÍ≥Ý, 100‚ÑÉÏóêÏÑú 30Î∂Ñ ÎèôÏïà Bond epitope retrieval Ïö©Ïï°(Vision BioSystems)ÏùÑ ÏǨÏö©ÌïòÏó¨ Ìï≠Ïõê Î≥µÍµ¨(antigen retrieval)Εº ÏàòÌñâÌïòÏòÄÎã§. ÎÇ¥Ïù∏Ïѱ Í≥ºÏÇ∞ÌôîÌö®ÏÜåÏùò ÌôúÏѱÏùÑ ÏñµÏÝúÌïòÍ∏∞ ÏúÑÌï¥ Í≥ºÏÇ∞Ìôî ÏàòÏÜå Ïö©Ïï°Ïóê 5Î∂ÑÍ∞Ñ Ï≤òζ¨ÌïòÏòÄÎã§. Í∑∏ ÌõÑ Ï°∞ÏßÅ ÏÝàÌé∏ÏùÑ CLDN-1Ïóê ÎåÄÌïú ÌÜÝÎźÏùò Îã§ÌÅ¥Î°Ý Ìï≠Ï≤¥(polyclonal antibody)(1:150, Abcam, Cambridge, UK)ÏôÄ Ìï®Íªò 15Î∂ÑÍ∞Ñ Ï£ºÏúÑ Ïò®ÎèÑ(ambient temperature)ÏóêÏÑú Î∞∞ÏñëÌïòÏòÄÎã§. ÎπÑÏò§Ìã¥(biotin)Ïù¥ ÏóÜÎäî Í≥ÝÏ∂îÎÉâÏù¥ Í≥ºÏÇ∞ÌôîÌö®ÏÜå(horseradish peroxicase)-ÎßÅϪ§(linker) Ìï≠Ï≤¥ ÏÝëÌï© ÏãúÏä§ÌÖúÏùÑ BondmaX ÏûêÎèô Ï°∞ÏßÅ ÏóºÏÉâÍ∏∞(Vision BioSystems)ÏôÄ Ìï®Íªò ÏǨÏö©ÌïòÏòÄÎã§. Î∞úÏÉâÏÝúΰúÎäî 1 mM 3,3‚Äô-Îã§Ïù¥ÏïÑÎØ∏ÎÖ∏Î≤§ÏßÄÎîò(diaminobenzidine), 50 mM Tris-HCl ÏôÑÏ∂©Ïï°(pH 7.6), Í∑∏ζ¨Í≥Ý 0.006% Í≥ºÏÇ∞ÌôîÏàòÏÜå Ïö©Ïï°ÏùÑ Î∞òÏùëÏãúϺú ÏÑ∏Ï≤ôÌïòÏòÄÍ≥Ý, hematoxylinÏúºÎ°ú ÎåÄÏ°∞ ÏóºÏÉâÏùÑ Ïã§ÏãúÌïòÏòÄÎã§. Ìëú준 ÏÝàÏ∞®Ïóê Îî∞Îùº Ï°∞ÏßÅ Ïä¨ÎùºÏù¥ÎìúΕº ÌÉàÏàòÏãúÌǧÍ≥Ý Ïª§Î≤Ñ Ïä¨Î¶ΩÏúºÎ°ú Î∞ÄÎ¥âÌïòÏòÄÎã§.
Ω¥Ïó≠Ï°∞ÏßÅÌôîÌïôÏóºÏÉâ Í≤∞Í≥ºÏùò ÌåêÎèÖÏóºÏÉâÍ≤∞Í≥ºÏùò ÌåêÎèÖÏùÄ 2ΙÖÏùò Î≥ëζ¨ÏÝÑΨ∏ÏùòÏóê ÏùòÌïòÏó¨ Í≥ºÍ±∞Ïùò Ï°∞ÏßÅÎ≥ëζ¨ÌïôÏÝÅ, ÏûÑÏÉÅÏÝÅ ÏÝïÎ≥¥ ÏóÜÏù¥ ÏãúÌñâÎêòÏóàÏúºÎ©∞ 200Î∞∞, 400Î∞∞ Í¥ëÌïôÌòÑÎØ∏Í≤Ω ÏÜåÍ≤¨ÌïòÏóêÏÑú ÌåêÎèÖÌïòÏòÄÎã§. CLDN-1 Ω¥Ïó≠Ï°∞ÏßÅÌôîÌïôÏóºÏÉâÏóêÏÑú ÏÑ∏Ìè¨ÎßâÏóê Î∂ÑΙÖÌïú Í∞àÏÉâÏùò Î∞òÏùëÏùÑ Î≥¥Ïùº Îïå ÏùòÎØ∏ ÏûàÎäî Í≤ÉÏúºÎ°ú ÌåêÎèÖÌïòÏòÄÎã§. CLDN-1Ïùò ÏÑ∏Ìè¨Îßâ ÏóºÏÉâ Í∞ïÎèÑÎäî 0~3ÍπåÏßÄ Î∞òÏÝïÎüâÏÝÅÏúºÎ°ú ͵¨Î∂ÑÎêòÏóàÎã§(0: negative; 1: weak; 2: moderate; 3: strong)(Fig. 1). 2ΙÖÏùò Î≥ëζ¨ ÏÝÑΨ∏ÏùòÎäî Í∞úÎ≥ÑÏÝÅÏúºÎ°ú ÏÝÑÏ≤¥ ÌôòÏûê Ïä¨ÎùºÏù¥ÎìúÏóê ÎåÄÌïú ÌåêÎèÖÏùÑ ÏúÑ Í∏∞ϧÄÏóê ÎßûÏ∂∞ ÏãúÌñâÌïòÏòÄÍ≥Ý, ÌåêÎèÖÎêú Í≤∞Í≥ºÎ•º ÎπÑ͵êÌïòÏó¨ ÏÑúΰú Îã§Î•∏ ÌåêÎèÖ Í≤∞Í≥ºÎ•º Î≥¥Ïù¥Îäî ÌôòÏûêÏùò Ïä¨ÎùºÏù¥ÎìúÏóê ÎåÄÌï¥ÏÑúÎäî Ïû¨ÌåêÎèÖÏùÑ ÏãúÌñâÌïòÏòÄÎã§. ÌܵÍ≥ÑÌïôÏÝÅÏù∏ ÎπÑ͵ê Î∂ÑÏÑùÏùÑ ÏúÑÌï¥ ÏóºÏÉâ Í≤∞Í≥ºÏùò ÌåêÏÝïÏùÑ Îëê Í∞úÏùò ͵∞ÏúºÎ°ú ÎÇòÎàÑÏñ¥ÏÑú 0, 1ÏùÑ ÏïΩÏñëÏѱ Î∞úÌòÑ͵∞(low), 2, 3ÏùÑ Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞(high)ÏúºÎ°ú ͵¨Î∂ÑÌïòÏòÄÎã§.
ÌܵÍ≥Ñ Î∂ÑÏÑùCLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Îùº ÌôòÏûêÏùò ÏûÑÏÉÅÎ≥ëÍ∏∞, Í≤ΩÎ∂Ä Î¶ºÌîÑÏÝà ÏÝÑÏù¥ Ïó¨Î∂Ä, Ïû¨Î∞úÍ≥ºÏùò ÏÉÅÍ¥ÄÍ¥ÄÍ≥ÑΕº chi-squareÏôÄ Fisher‚Äôs extract, Í∑∏ζ¨Í≥Ý linear by linear association Í≤ÄÏÝïÏúºÎ°ú Î∂ÑÏÑùÌïòÏòÄÍ≥Ý, ÏúÝÏùòÏàòϧÄÏùÑ pÔºú0.05Εº ÏùòÎØ∏ ÏûàÎäî Í≤ÉÏúºÎ°ú ÌïòÏòÄÎã§. Í≤ΩÎ∂Ä Î¶ºÌîÑÏÝà ÏÝÑÏù¥ÏôÄ Ïó∞Í¥ÄÏѱÏù¥ ÏûàÎäî ÏúÑÌóò ÏöîÏù∏ÏùÑ Ï∞æÍ∏∞ ÏúÑÌï¥ logistic regression Î∂ÑÏÑùÎ≤ïÏùÑ ÏǨÏö©ÌñàÎã§. ÎòêÌïú ÏÉùÏ°¥ Í∏∞Í∞ÑÏùÄ Kaplan-MeierÎ≤ïÏùÑ Ïù¥Ïö©ÌïòÏòÄÍ≥Ý, CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ÏÉùÏ°¥ Í∏∞Í∞ÑÏùò Ï∞®Ïù¥Îäî log-rankÎ≤ïÏùÑ Ïù¥Ïö©ÌïòÏó¨ ÎπÑ͵ê Î∂ÑÏÑùÌïòÏòÄÎã§.
Í≤∞ Í≥ºÏÝÑÏ≤¥ ÌôòÏûêÎäî 91ΙÖÏúºÎ°ú Î≥ëÎ≥ÄÏùò ÏõêÎ∞ú Î∂ÄÏúÑÎäî ͵¨Í∞ï 23Ïòà, ͵¨Ïù∏Îëê 15Ïòà, ÌõÑÎëê 33Ïòà, ÌïòÏù∏Îëê 13Ïòà, ÎπÑÎ∂ÄÎπÑÎèô 7ÏòàÏòÄÎã§(Table 1). ÏûÑÏÉÅ Î≥ëÍ∏∞Îäî 8th American Joint Committee on Cancer staging systemÏóê Îî∞Îùº Í≤∞ÏÝïÌïòÏòÄÎã§.
ÏѱÎ≥Ñ Î∞è Ïó∞ÎÝπÍ≥º CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÏÝÑÏ≤¥ ÌôòÏûê 91Î™Ö Ï§ë ÎÇ®Ïûê 73ΙÖ(80.2%), Ïó¨Ïûê 18ΙÖ(19.8%)Ïù¥ÏóàÏúºÎ©∞ ÌèâÍ∑Ý ÎÇòÏù¥Îäî 65ÏÑ∏(31~85ÏÑ∏)ÏòÄÎã§. CLDN-1ÏùÄ 73ÏòàÏùò ÎÇ®Ïûê ϧë 63Ïòà(86%)ÏóêÏÑú Í∞ïÌïú ÏàòϧÄÏùò Î∞úÌòÑÏùÑ Î≥¥ÏòÄÍ≥Ý, ÎÇòή∏ÏßÄ 10Ïòà(14%)ÏóêÏÑúÎäî ÏïΩÌïú ÏàòϧÄÏùò Î∞úÌòÑÏùÑ ÎÇòÌÉÄÎÉàÎã§. Ïó¨ÏûêÏóêÏÑúÎäî 18Ïòà ϧë 9Ïòà(50%)ÏóêÏÑú Í∞ïÌïú Î∞úÌòÑ, ÎÇòή∏ÏßÄ 9Ïòà(50%)ÏóêÏÑú ÏïΩÌïú Î∞úÌòÑÏùÑ Î≥¥ÏòÄÎã§. Îî∞ÎùºÏÑú ÎÇ®ÏѱÏóêÏÑú CLDN-1Ïùò Î∞úÌòÑÏù¥ Îçî Í∞ïÌïòÍ≤å ÎÇòÌÉÄÎÇòÎäî Í≤∞Í≥ºÎ•º Î≥¥ÏòÄÍ≥Ý, Ïù¥Îäî ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏùòÎØ∏ ÏûàÎäî Í≤∞Í≥ºÎ•º Î≥¥ÏòÄÎã§(p=0.002). Ïó∞ÎÝπÎ≥ÑΰúÎäî 60ÏÑ∏ Ïù¥ÏÉÅÏù∏ ͵∞Ïù¥ 57Ïòà(62.6%), 60ÏÑ∏ ÎØ∏ÎßåÏù∏ ͵∞Ïù¥ 34Ïòà(37.4%)Ïù¥ÏóàÎã§. 60ÏÑ∏ Ïù¥ÏÉÅÏù∏ ͵∞ÏóêÏÑú CLDN-1Ïùò Î∞úÌòÑÏùÄ 57Ïòà ϧë 46Ïòà(80.7%)ÏóêÏÑú Í∞ïÌïú Î∞úÌòÑ, ÎÇòή∏ÏßÄ 11Ïòà(19.3%)ÏóêÏÑú ÏïΩÌïú Î∞úÌòÑÏùÑ Î≥¥ÏòÄÍ≥Ý 60ÏÑ∏ ÎØ∏ÎßåÏù∏ ͵∞ÏóêÏÑúÎäî 34Ïòà ϧë 26Ïòà(76.5%)ÏóêÏÑú Í∞ïÌïú Î∞úÌòÑ, ÎÇòή∏ÏßÄ 8Ïòà(23.5%)ÏóêÏÑú ÏïΩÌïú Î∞úÌòÑÏùÑ ÎÇòÌÉÄÎÉàÎã§. Ïó∞ÎÝπÎ≥Ñ Îëê ͵∞Í≥º CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑ Í∞ÑÏóê ÌܵÍ≥ÑÏÝÅ ÏúÝÏùòÏѱÏùÄ ÏóÜÏóàÎã§(p=0.631)(Table 1).
CLDN-1Ïùò Ω¥Ïó≠Ï°∞ÏßÅÌôîÌïôÏÝÅ Î∞úÌòÑ ÏñëÏÉÅÏÝÑÏ≤¥ ÎëêÍ≤ΩÎ∂ÄÏïî 91Ïòà ϧë 72Ïòà(79%)Í∞Ä Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞Ïóê ÏÜçÌïòÏòÄÍ≥Ý, ÏõêÎ∞ú Î∂ÄÏúÑÎ≥Ñΰú ͵¨Í∞ï 23Ïòà ϧë 14Ïòà(61%), ͵¨Ïù∏Îëê 15Ïòà ϧë 11Ïòà(73%), ÌõÑÎëê 33Ïòà ϧë 28Ïòà(85%), ÌïòÏù∏Îëê 13Ïòà ϧë 12Ïòà(92%), ÎπÑÎ∂ÄÎπÑÎèô 7Ïòà ϧë 7Ïòà(100%)ÏóêÏÑú Í∞ïÏñëÏѱ Î∞úÌòÑÏùÑ Î≥¥ÏòÄÎã§(Table 1). Ι®ÎìÝ ÏõêÎ∞ú Î∂ÄÏúÑÏóêÏÑú CLDN-1Ïù¥ Í∞ïÌïòÍ≤å Î∞úÌòÑÎêòÎäî Í≤ΩÏö∞Í∞Ä Î≥¥Î㧠Ïö∞ÏÑ∏Ìïú Í≤ÉÏúºÎ°ú ÎÇòÌÉÄÎǨÍ≥Ý, Í∑∏ ϧë ͵¨Í∞ïÏïîÍ≥º ÎπÑÎ∂ÄÎπÑÎèôÏïîÏùÑ ÏÝúÏô∏Ìïú ͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî ÏÑ∏ ͵∞ÏóêÏÑúÎäî CLDN-1 Í∞ïÏñëÏѱ ͵∞Ïù¥ 61Ïòà ϧë 51Ïòà(83%)ΰú ͵¨Í∞ïÏïîÏùò 61%Î≥¥Î㧠ÎπÑ͵êÏÝÅ ÎÜíÏùÄ Î∞úÌòÑÏú®ÏùÑ Î≥¥ÏòÄÎã§.
CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÏôÄ ÏûÑÏÉÅÎ≥ëζ¨ÌïôÏÝÅ ÌäπÏѱÍ≥ºÏùò ÏÉÅÍ¥ÄÍ¥ÄÍ≥ÑCLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ Ï¢ÖÏñëÏùò ζºÌîÑ관 Ïπ®Ïú§ÏùÄ CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑÏóêÏÑú 23Ïòà(96%), ÏïΩÏñëÏѱ Î∞úÌòÑÏóêÏÑú 1Ïòà(4%)ΰú CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞ÏóêÏÑú ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌïòÍ≤å ÎÜíÏùÄ Ï¢ÖÏñëÏùò ζºÌîÑ관 Ïπ®Ïú§ÏùÑ Î≥¥ÏòÄÎã§(p=0.019). Í∑∏Îü¨ÎÇò ÎåÄÏÉÅÏùÑ ÏõêÎ∞ú Î∂ÄÏúÑÎ≥Ñΰú ÎÇòÎàÑÏñ¥ ͵¨Í∞ïÏïî, ͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî Í∞ÅÍ∞ÅÏóêÏÑú CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ζºÌîÑ관 Ïπ®Ïú§Ïóê ÎåÄÌï¥ ÎπÑ͵êÌïòÏòÄÏùÑ ÎïåÎäî, Îѧ ͵∞ Ι®Îëê ÌܵÍ≥ÑÌïôÏÝÅÏúºÎ°ú ÏúÝÏùòÌïú Ï∞®Ïù¥Î•º Î≥¥Ïù¥ÏßÄ ÏïäÏïòÎã§(͵¨Í∞ïÏïî: p=1.000, ͵¨Ïù∏ÎëêÏïî: p=0.231, ÌõÑÎëêÏïî: p=0.556, ÌïòÏù∏ÎëêÏïî: p=0.462). ÎπÑÎ∂ÄÎπÑÎèôÏïîÏóêÏÑúÎäî 7Ïòà ϧë 7Ïòà Ι®Îëê Í∞ïÏñëÏѱ Î∞úÌòÑÏùÑ Î≥¥ÏòÄÍ∏∞ ÎïåΨ∏Ïóê ÏïΩÏñëÏѱ Î∞úÌòÑ͵∞Ïù¥ Ï°¥Ïû¨ÌïòÏßÄ ÏïäÏïÑ Îëò ÏǨÏù¥Ïùò Ïó∞Í¥ÄÏѱ Î∂ÑÏÑùÏù¥ Î∂àÍ∞ÄÌïòÏòÄÎã§(Table 2). ÏõêÎ∞ú Î∂ÄÏúÑ Ï§ë ͵¨Í∞ïÏïîÏóêÏÑúÎäî CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ζºÌîÑ관 Ïπ®Ïú§Ïóê ÎåÄÌï¥ ÌܵÍ≥ÑÏÝÅ ÏúÝÏùòÏѱÏùÑ Î≥¥Ïù¥ÏßÄ ÏïäÏïòÏúºÎÇò(p=1.000) ÏïûÏÑú CLDN-1Ïùò ÎÜíÏùÄ Î∞úÌòÑÏú®ÏùÑ Î≥¥ÏòÄÎçò ͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî ÏÑ∏ ͵∞ÏùÑ ÎåÄÏÉÅÏúºÎ°ú ÎπÑ͵êÌïòÏòÄÏùÑ ÎïåÎäî CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞ÏóêÏÑú ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌïòÍ≤å ÎÜíÏùÄ Ï¢ÖÏñëÏùò ζºÌîÑ관 Ïπ®Ïú§ÏùÑ Î≥¥ÏòÄÎã§(p=0.026).
CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ÏûÑÏÉÅÎ≥ëζ¨ÌïôÏÝÅ ÏöîÏù∏Îì§Í≥ºÏùò Ïó∞Í¥ÄÏѱ Î∂ÑÏÑùÏóêÏÑúÎäî ÏÝÑÏ≤¥ ÎëêÍ≤ΩÎ∂ÄÏïî 91ÏòàÏóêÏÑú T Î≥ëÍ∏∞, N Î≥ëÍ∏∞, Ïû¨Î∞úÍ≥º CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÎäî ÌܵÍ≥ÑÌïôÏÝÅÏúºÎ°ú ÏúÝÏùòÌïú ÏÉÅÍ¥ÄÍ¥ÄÍ≥ÑΕº Î≥¥Ïù¥ÏßÄ ÏïäÏïòÎã§(pÔºû0.05)(Table 1). ÎòêÌïú ÏõêÎ∞ú Î∂ÄÏúÑ Ï§ë ͵¨Í∞ïÏïî 23ÏòàÏôÄ, ͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî 61ÏòàΕº ÎåÄÏÉÅÏúºÎ°ú Ìïú Î∂ÑÏÑùÏóêÏÑúÎèÑ ÏúÑÏùò ÏöîÏù∏Îì§Í≥º CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÎäî ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌïú ÏÉÅÍ¥ÄÍ¥ÄÍ≥ÑΕº Î≥¥Ïù¥ÏßÄ ÏïäÏïòÎã§(pÔºû0.05). CLDN-1 Î∞úÌòÑ ÏÝïÎèÑ Ïù∏ÏûêÏôÄ Ìï®Íªò ÏûÑÏÉÅÎ≥ëζ¨ÌïôÏÝÅ ÏöîÏù∏Îì§ Ï§ë Í≤ΩÎ∂Ä Î¶ºÌîÑÏÝà ÏÝÑÏù¥Ïùò ÏúÑÌóòÏöîÏù∏ÏùÑ Ï∞æÍ∏∞ ÏúÑÌïú Îã§Î≥ÄÎüâ Î∂ÑÏÑùÏóêÏÑúÎäî T Î≥ëÍ∏∞, ζºÌîÑ관 Ïπ®Ïú§ Ïó¨Î∂ÄÍ∞Ä Í≤ΩÎ∂Ä Î¶ºÌîÑÏÝà ÏÝÑÏù¥Ïóê ϧëÏöîÌïú Ïù∏ÏûêÏòÄÎã§(T stage: odds ratio=1.899, lymphatic invasion: odds ratio=4.684) (Table 3).
ÏÉùÏ°¥Ïú® Î∂ÑÏÑùÎ≥∏ Ïó∞͵¨Ïùò HNSCC ÌôòÏûê 91ΙÖÏóêÏÑú Kaplan-Meier Î∞©Î≤ïÏóê ÏùòÌïú ÏÝÑÏ≤¥ ÏÉùÏ°¥Ïú®(overall survival)ÏùÄ 3ÎÖÑÏß∏Ïóê 64%, 5ÎÖÑÏß∏Ïóê 53%ÏòÄÎã§. ÏßàÎ≥ë ÌäπÏù¥ ÏÉùÏ°¥Ïú®(disease specific survival)ÏùÄ 3ÎÖÑÏß∏Ïóê 78%, 5ÎÖÑÏß∏Ïóê 70%ÏòÄÎã§. CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Îùº ÏÉùÏ°¥Ïú®Ïóê Ï∞®Ïù¥Í∞Ä ÏûàÏóàÍ≥Ý CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞Ïùò ÏÝÑÏ≤¥ ÏÉùÏ°¥Ïú®Ïù¥ 3ÎÖÑÏß∏Ïóê 53%, 5ÎÖÑÏß∏Ïóê 49%ÏòÄÍ≥Ý, CLDN-1 ÏïΩÏñëÏѱ Î∞úÌòÑ͵∞ ÏÝÑÏ≤¥ ÏÉùÏ°¥Ïú® 3ÎÖÑÏß∏Ïóê 74%, 5ÎÖÑÏß∏Ïóê 68%ΰú CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞Ïùò ÏÝÑÏ≤¥ ÏÉùÏ°¥Ïú®Ïù¥ ÏïΩÏñëÏѱ Î∞úÌòÑ͵∞Î≥¥Î㧠ÏúÝÏùòÌïòÍ≤å ÎÇÆÏïòÎã§(p=0.022)(Fig. 2). ÏõêÎ∞ú Î∂ÄÏúÑÎ≥Ñ CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ÏÝÑÏ≤¥ ÏÉùÏ°¥Ïú®Ïùò Ï∞®Ïù¥Îäî ͵¨Í∞ïÏïîÏóêÏÑúÎßå ÌܵÍ≥ÑÌïôÏÝÅ ÏúÝÏùòÏѱÏù¥ ÏûàÏóàÏúºÎ©∞, ÎÇòή∏ÏßÄ ÏõêÎ∞ú Î∂ÄÏúÑÏóêÏÑúÎäî ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌïòÏßÄ ÏïäÏïòÎã§(͵¨Í∞ïÏïî: p=0.004, ͵¨Ïù∏ÎëêÏïî: p=0.640, ÌõÑÎëêÏïî: p=0.589, ÌïòÏù∏ÎëêÏïî: p=0.260). ÎòêÌïú ͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî ÏÑ∏ ͵∞ÏùÑ ÎåÄÏÉÅÏúºÎ°ú Î∂ÑÏÑùÌïòÏòÄÏùÑ ÎïåÏóêÎèÑ ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌïòÏßÄ ÏïäÏïòÎã§(p=0.941). ÏßàÎ≥ë ÌäπÏù¥ ÏÉùÏ°¥Ïú®(disease specific survival)ÏùÄ 3ÎÖÑÏß∏Ïóê 78%, 5ÎÖÑÏß∏Ïóê 70%ÏòÄÎã§. CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Îùº ÏßàÎ≥ë ÌäπÏù¥ ÏÉùÏ°¥Ïú®Ïóê Ï∞®Ïù¥Í∞Ä ÏûàÏóàÍ≥Ý CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞Ïùò ÏßàÎ≥ë ÌäπÏù¥ ÏÉùÏ°¥Ïú®Ïù¥ 5ÎÖÑÏß∏Ïóê 56%ÏòÄÍ≥Ý, CLDN-1 ÏïΩÏñëÏѱ Î∞úÌòÑ͵∞ ÏÝÑÏ≤¥ ÏÉùÏ°¥Ïú® 5ÎÖÑÏß∏Ïóê 89%ΰú CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞Ïùò ÏßàÎ≥ë ÌäπÏù¥ ÏÉùÏ°¥Ïú®Ïù¥ ÏïΩÏñëÏѱ Î∞úÌòÑ͵∞Î≥¥Î㧠ÏúÝÏùòÌïòÍ≤å ÎÇÆÏïòÎã§(p=0.044).
Í≥Ý Ï∞∞ÏÝïÏÉÅ ÏÉÅÌîºÏ°∞ÏßÅÍ≥º ÎßàÏ∞¨Í∞ÄÏßÄΰú ÏÉÅÌîºÏÑ∏Ìè¨ Í∏∞Ïõê Ï¢ÖÏñëÏùò ÌäπÏßï ϧë ÌïòÎÇòÎäî ÏÉÅÌîºÏÑ∏Ìè¨Í∞Ä Î∞ÄÏ∞©Ïó∞ÏÝë, Î∂ÄÏ∞©Ïó∞ÏÝë(adherens junction), Îç∞Ïä§Î™®Ï¢Ä(desmosome)ÏúºÎ°ú ͵¨ÏѱÎêòÎäî Ïó∞Í≤∞Î≥µÌï©Ï≤¥Î•º ÌܵÌï¥ Ï£ºÎ≥Ä ÏÑ∏Ìè¨ÏôÄ Î∞ÄÏ∞©ÌïòÏó¨ Îã®Îã®Ìûà Î∂ÄÏ∞©ÎêòÏñ¥ ÏûàÎã§Îäî ÏÝêÏù¥Îã§[8]. Ïó∞Í≤∞Î≥µÌï©Ï≤¥ ϧë Î∂ÄÏ∞©Ïó∞ÏÝëÍ≥º Îç∞Ïä§Î™®Ï¢ÄÏù¥ Ï£ºÎ≥Ä ÏÑ∏Ìè¨ÏôÄÏùò Í∏∞Í≥ÑÏÝÅÏù∏ ÏÝëÏ∞© Í∏∞Îä•ÏùÑ Îã¥ÎãπÌïòÎäî Î∞òΩ¥, Î∞ÄÏ∞©Ïó∞ÏÝëÏùÄ ÏÑ∏Ìè¨Ï∏µ(cell sheet)Ïùò Îã®Îã®Ìïú Î¥âÌï©Ïóê ÌïÑÏàòÏÝÅÏù¥Î©∞, ÏÑ∏Ìè¨Ïùò Í∑πÏѱ ÏúÝÏßÄ, ÏÑ∏Ìè¨ Ï£ºÏúÑÏóêÏÑú ÏùºÏñ¥ÎÇòÎäî ΨºÏßàÏùò ÏàòÏÜ°, Ïö¥Î∞ò Ï°∞ÏÝà Î∞è Ïû•Î≤Ω Í∏∞Îä•Ïóê ϧëÏöîÌïú Ïó≠ÌïÝÏùÑ ÌïúÎã§[9]. ÌïúÌé∏, ÏïîÏùò Ï£ºÎ≥Ä Ïπ®ÏäµÍ≥º ÏÝÑÏù¥ Í≥ºÏÝïÏùÄ ÏÑ∏Ìè¨ÏôÄ ÏÑ∏Ìè¨ Í∞Ñ(cell-to-cell), ÏÑ∏Ìè¨ÏôÄ ÏÑ∏Ìè¨ Ïô∏ Í∏∞Ïßà Í∞ÑÏùò(cell-to-extracellular matrix) ÏúÝÏ∞©(adhesion)Í≥º Î∞ÄÏÝëÌïú Í¥ÄÎÝ®ÏùÑ Í∞ÄÏßÄÍ≥Ý ÏûàÎã§[10,11]. Ïù¥ ϧë Ï¢ÖÏñë ÏÑ∏Ìè¨ÏôÄ Í∏∞Ïßà Í∞ÑÏùò ÏÉÅÌò∏ ÏãÝÌò∏ ÏÝÑÎã¨ÏùÄ ÌäπÌûà Ï¢ÖÏñë ÏÑ∏Ìè¨Í∞Ä ÌäπÏÝï Ïû•Í∏∞Ïóê ÏïàÏ∞©ÌïòÏó¨ ÏѱÏû•ÌïòÎäî Îç∞ ϧëÏöîÌïòÎã§[12]. Ï¢ÖÏñëÏÑ∏Ìè¨Îäî ÌùîÌûà ÏÑ∏Ìè¨ Î∂ÑÌôî Î∞è Í∑πÏѱÏùò Í∞êÏÜåΕº Î≥¥Ïù¥Î©¥ÏÑú Î∞ÄÏ∞©Ïó∞ÏÝëÏùò Í∏∞Îä•Ïù¥ ÎπÑÏÝïÏÉÅÏÝÅÏúºÎ°ú ÎÇòÌÉÄÎÇúÎã§[13,14]. Î∞ÄÏ∞©Ïó∞ÏÝëÏùò Í∏∞Îä• ÏÜêÏã§ÏùÄ ÏÑ∏Ìè¨ Îǥΰú ÏòÅÏñëÎ∂ÑÏùò ÌôïÏÇ∞ÏùÑ Ïö©Ïù¥ÌïòÍ≤å ÌïòÏó¨ Ï¢ÖÏñë ÏÑ∏Ìè¨Ïùò ÏѱÏû•ÏùÑ Ï¥âÏßÑÏãúÌÇ®Îã§. ÎòêÌïú Ï¢ÖÏñë ÏÑ∏Ìè¨Ïùò Î∂ÑÌôî Î∞è Í∑πÏѱÏùò Í∞êÏÜåÎäî Ï¢ÖÏñë ÏÑ∏Ìè¨Í∞Ä ÏõêÎ∞ú Î∂ÄÏúÑÏóêÏÑú Îñ®Ïñ¥ÏÝ∏ ÎÇòÏôÄ Î¶ºÌîÑÍ≥Ñ ÎòêÎäî ÌòàΕòΕº ÌÉÄÍ≥Ý Ïù¥ÎèôÌïòÏó¨ ÌäπÏÝï Ïû•Í∏∞Ïóê ÏÝÑÏù¥ÎêòÎäî Îç∞ Í∏∞Ïó¨ÌïúÎã§[15,16]. Ïù¥Îäî Ïó∞Í≤∞Î≥µÌï©Ï≤¥Î•º Ïù¥Î£®Îäî ÏÑ∏Ìè¨ Í∞Ñ Î∂ÄÏ∞© Ïû•ÏπòÍ∞Ä ÏïîÏÑ∏Ìè¨Îì§Ïùò ÌôúÏѱÏùÑ Í∞ïÎÝ•ÌïòÍ≤å Ï°∞ÏÝàÌïòÍ≥Ý, ÏßàÎ≥ë ÏßÑÌñâÏóê ϧëÏöîÌïú Ïó≠ÌïÝÏùÑ ÌïÝ Ïàò ÏûàÏùåÏùÑ ÏãúÏǨÌïúÎã§[17,18]. ÎòêÌïú, ϵúÍ∑º Ïó∞͵¨Îì§ÏùÄ Ïù¥Îü¨Ìïú ÏÑ∏Ìè¨ Í∞Ñ Î∂ÄÏ∞© Ïû•ÏπòÍ∞Ä ÏÑ∏Ìè¨ Ï¶ùÏãù Î∞è Î∂ÑÌôîΕº Ï°∞ÏÝàÌïòÎäî Îç∞ÏóêÎèÑ Í¥ÄÏó¨ÌïÝ Ïàò ÏûàÏùåÏùÑ ÏÝúÏãúÌïòÏòÄÎã§[2].
ClaudinÏùÄ Î∞ÄÏ∞©Ïó∞ÏÝëÏùò Ï£ºÏöî Í≥®Í≤©ÏùÑ ÌòïÏѱÌïòÎäî ÎßâÎã®Î∞±Ïßàΰú claudinÏùò Î∞úÌòÑ ÏÝïÎèÑÏùò Î≥ÄÌôîÏôÄ Íµ¨Ï°∞ÏÝÅ Î≥ÄÌôîÎäî ÏÑ∏Ìè¨Îßâ ÌëúΩ¥ÏóêÏÑú Î∞ÄÏ∞©Ïó∞ÏÝëÏùò ͵¨Ï°∞ÏôÄ Í∏∞Îä•Ïóê ÏßÅÏÝëÏÝÅÏù∏ ÏòÅÌñ•ÏùÑ ÎØ∏ÏπúÎã§[19]. ClaudinÏùÄ Îã§ÏñëÌïú ÏïÖÏѱ Ï¢ÖÏñëÏóêÏÑú ÎπÑÏÝïÏÉÅÏÝÅÏúºÎ°ú Î∞úÌòÑÎêòΩ∞, Ïù¥Îäî Î∞ÄÏ∞©Ïó∞ÏÝëÏùò ÏÝïÏÉÅÏÝÅÏù∏ ͵¨Ï°∞ÏôÄ Í∏∞Îä•ÏùÑ Î≥ÄÌôîÏãúϺú Ï¢ÖÏñë ÏÑ∏Ìè¨Ïùò Ïπ®ÏäµÏѱÍ≥º ÏÝÑÏù¥ Í∞ÄÎä•ÏѱÏùÑ Ï¥âÏßÑÏãúÌÇ®Îã§[20]. ClaudinÏùÄ ÌòÑÏû¨ÍπåÏßÄ 24Í∞úÏùò ÏïÑÌòïÏù¥ Î∞ùÌòÄÏ°åÏúºÎ©∞, ÏÝïÏÉÅ ÏÑ∏Ìè¨Îäî ÌäπÏßïÏÝÅÏúºÎ°ú Ïó¨Îü¨ claudin Îã®Î∞±ÏùÑ Î∞úÌòÑÌïòÏßÄÎßå Ïñ¥Îñ§ ÏïÑÌòïÏùò claudinÏùÄ Ï°∞ÏßÅ ÌäπÏù¥ÏÝÅÏù∏ Î∂ÑÌè¨Î•º Î≥¥Ïù∏Îã§. ÏòàΕº Îì§Ïñ¥, claudin-1ÏùÄ Ìèê, Í∞Ñ, ÏãÝÏû• Ι®ÎëêÏóêÏÑú Î∞úÌòÑÎêòÍ≥Ý, claudin-2Îäî ÌèêÏóêÏÑúÎäî Î∞úÌòÑÎêòÏßÄ ÏïäÍ≥Ý Í∞Ñ, ÏãÝÏû•ÏóêÏÑúÎäî Î∞úÌòÑÎêòÎäî Î∞òΩ¥, claudin-4Îäî Ìèê, ÏãÝÏû•ÏóêÏÑúÎäî Î∞úÌòÑÎêòÍ≥Ý Í∞ÑÏóêÏÑúÎäî Î∞úÌòÑÎêòÏßÄ ÏïäÎäîÎã§[21]. ÎòêÌïú Í∞ôÏùÄ ÏïÑÌòïÏùò claudinÏù¥ÎçîÎùºÎèÑ Îã§ÏñëÌïú ÏïîÏóêÏÑú Í∞ÅÍ∏∞ Îã§Î•∏ Î∞úÌòÑ ÏñëÏÉÅÏùÑ Î≥¥Ïù∏Îã§Îäî Ïó∞͵¨ Í≤∞Í≥ºÍ∞Ä Ïù¥ÎØ∏ Ïó¨Îü¨ ÎֺΨ∏ÏóêÏÑú ÏïåÎݧÏÝ∏ ÏûàÎã§. ÏòàΕº Îì§Ïñ¥, CLDN-1ÏùÄ ÎåÄÏû•Ïïî, ÏûêÍ∂ÅÍ≤ΩÎ∂ÄÏïî, ÏúÑÏïî, Í∞ëÏÉÅÏÑÝÏïî, ÏöîΰúÏÉÅÌîºÏïî Îì±ÏóêÏÑú Î∞úÌòÑÏù¥ ϶ùÍ∞ÄÎêú ÏñëÏÉÅÏùÑ Î≥¥ÏòÄÍ≥Ý[22], ÏúÝÎ∞©Ïïî, ÏÝÑζΩÏÑÝÏïî, Í∞ÑÏÑ∏Ìè¨ÏïîÏóêÏÑúÎäî Î∞úÌòÑÏù¥ Í∞êÏÜåÎêú ÏñëÏÉÅÏùÑ Î≥¥ÏòÄÎã§[12,23,24]. Ïù¥Î•º ÌܵÌï¥ÏÑú claudinÏù¥ Ï°∞ÏßÅ ÌäπÏù¥ÏÝÅ Í∏∞Îä•ÏùÑ Í∞ÄÏßà Ïàò ÏûàÏúºÎ©∞ claudinÏù¥ Í∞ÄÏßÄÎäî Ïó¨Îü¨ ÏïîÏóêÏÑúÏùò Ïó≠ÌïÝÏù¥ ÏïîÏÑ∏Ìè¨Ïùò ÏúÝÌòï Î∞è Ïïî Ï£ºÎ≥Ä ÌôòÍ≤ΩÏóê Îî∞Îùº Îã§Î•º Ïàò ÏûàÏùåÏùÑ Ïïå Ïàò ÏûàÎã§[2]. ÎëêÍ≤ΩÎ∂ÄÏïîÏóêÏÑúÎèÑ claudinÏùò Î∞úÌòÑ ÏñëÏÉÅÏóê ÎåÄÌïú Ïó¨Îü¨ Ïó∞͵¨Í∞Ä Ïù¥Î£®Ïñ¥ÏÝ∏ÏôîÎã§. Nelh≈±bel Îì±[1]ÏùÄ ÎëêÍ≤ΩÎ∂Ä Ìé∏ÌèâÏÑ∏Ìè¨ÏïîÏóêÏÑúÏùò claudin ÏïÑÌòïÏóê Îî∞Ε∏ Î∞úÌòÑ ÏñëÏÉÅÏùÑ Î∂ÑÏÑùÌïú Ïó∞͵¨Î•º Î≥¥Í≥ÝÌñàÎã§. Claudin 24Í∞ú ÏïÑÌòï ϧëÏóêÏÑú claudin-1, 2, 3, 4, 7, 8, 10Ïóê ÎåÄÌï¥ Ï°∞ÏǨÌïòÏòÄÍ≥Ý, Í∑∏ ϧë claudin-1, 2, 7 ÏÑ∏ ÏúÝÌòïÏù¥ ÏÝïÏÉÅ ÏÉÅÌîºÏ°∞ÏßÅÍ≥º ÎπÑ͵êÌïòÏó¨ Ìé∏ÌèâÏÑ∏Ìè¨ÏïîÏ¢Ö Ï°∞ÏßÅÏóêÏÑúÏùò Î∞úÌòÑ ÏñëÏÉÅÏóêÏÑú ÏúÝÏùòÎØ∏Ìïú Ï∞®Ïù¥Î•º Î≥¥ÏòÄÎã§. ÎëêÍ≤ΩÎ∂Ä Ìé∏Ìèâ ÏÑ∏Ìè¨ÏïîÏùÄ claudin-1Í≥º claudin-7Ïùò Î∞úÌòÑÏù¥ ϶ùÍ∞ÄÌïú Î∞òΩ¥ claudin-2Ïùò Î∞úÌòÑÏùÄ ÏúÝÏùòÌïòÍ≤å ÏïΩÌïú Í≤ÉÏúºÎ°ú ÎÇòÌÉÄÎǨÎã§.
Î≥∏ Ïó∞͵¨ÏóêÏÑúÎäî ͵¨Í∞ïÏïî, ͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî, Î∂ÄÎπÑÎèôÏïîÏùÑ Ìè¨Ìï®ÌïòÏó¨ Ïó¨Îü¨ ÎëêÍ≤ΩÎ∂ÄÏïî ͵∞ÏóêÏÑú CLDN-1Ïùò Î∞úÌòÑ ÏñëÏÉÅÏóê ÎåÄÌï¥ Ï°∞ÏǨÌïòÏòÄÎã§. ÏÝÑÏ≤¥Î•º ÎåÄÏÉÅÏúºÎ°ú ÌïòÏòÄÏùÑ Îïå, Í∑∏ζ¨Í≥Ý Í∞ÅÍ∞ÅÏùò ÏõêÎ∞ú Î∂ÄÏúÑÏóê ÎåÄÌï¥ÏÑú Ι®Îëê CLDN-1Ïùò Í∞ïÌïú Î∞úÌòÑÏù¥ Ïö∞ÏÑ∏Ìïú Í≤ÉÏúºÎ°ú ÎÇòÌÉÄÎǨÎã§. ÌäπÌûà Ïù¥ÎØ∏ CLDN-1Ïóê ÎåÄÌï¥ Ïó¨Îü¨ Ïó∞͵¨Í∞Ä Ïù¥Î£®Ïñ¥ÏßÑ Íµ¨Í∞ïÏïîÏóêÏÑúÎ≥¥Î㧠͵¨Ïù∏ÎëêÏïî, ÌõÑÎëêÏïî, ÌïòÏù∏ÎëêÏïî ÏÑ∏ ͵∞ÏóêÏÑú CLDN-1 Í∞ïÏñëÏѱ ͵∞Ïù¥ 61Ïòà ϧë 51Ïòà(83%)ΰú ÎπÑ͵êÏÝÅ ÎÜíÏùÄ Î∞úÌòÑÏú®ÏùÑ Î≥¥ÏòÄÎã§. Ï¢ÖÏñëÏùò ÏûÑÏÉÅÎ≥ëζ¨ÌïôÏÝÅ ÌäπÏßï ϧëÏóêÏÑúÎäî CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞ÏóêÏÑú ζºÌîÑ관 Ïπ®Ïú§Ïù¥ Îçî ÎπàÎ≤àÌïú Í≤ÉÏúºÎ°ú ÎÇòÌÉÄÎǨÏúºÎ©∞, ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌñàÎã§. ÎòêÌïú Í∞ÅÍ∞ÅÏùò ÏõêÎ∞ú Î∂ÄÏúÑÎ≥Ñ Î∂ÑÏÑùÏóêÏÑúÎäî ÌܵÍ≥ÑÏÝÅ ÏúÝÏùòÏѱÏùÑ ÏñªÏßÄ Î™ªÌïòÏòÄÏúºÎÇò, ͵¨Ïù∏Îëê, ÌõÑÎëê, ÌïòÏù∏Îëê ÏÑ∏ ͵∞ÏùÑ ÎåÄÏÉÅÏúºÎ°ú Ìïú Î∂ÑÏÑùÏóêÏÑúÎäî CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê Îî∞Ε∏ ζºÌîÑ관 Ïπ®Ïú§ Ïó¨Î∂ÄÍ∞Ä ÌܵÍ≥ÑÏÝÅÏúºÎ°ú ÏúÝÏùòÌïú Ï∞®Ïù¥Î•º Î≥¥ÏòÄÎã§. Ïù¥Ïóê ÎåÄÌï¥ÏÑúÎäî Ìñ•ÌõÑ Í∞Å ÏõêÎ∞ú Î∂ÄÏúÑÏóê ÎåÄÌï¥, Í∑∏ζ¨Í≥Ý ÌäπÌûà Ïù∏ÌõÑÎëêÎ∂ÄÏúÑÏóê ÎåÄÌï¥ Îçî ÎßéÏùÄ ÌëúÎ≥∏ÏùÑ ÎåÄÏÉÅÏúºÎ°ú ÌïòÎäî Ïó∞͵¨Í∞Ä ÌïÑÏöîÌïÝ Í≤ÉÏúºÎ°ú ÏǨΣåÎêúÎã§. ÎòêÌïú Î≥∏ Ïó∞͵¨ÏóêÏÑúÎäî ÎÇ®ÏѱÏóêÏÑú CLDN-1Ïùò Î∞úÌòÑ ÏÝïÎèÑÍ∞Ä Îçî Í∞ïÌïú Í≤ÉÏúºÎ°ú ÎÇòÌÉÄÎǨÏúºÎÇò, ÎπÑÏä∑Ìïú Îã§Î•∏ Ïó∞͵¨ Í≤∞Í≥ºÏóêÏÑúÎäî ÏѱÎ≥ÑÏóê Îî∞Ε∏ CLDN-1 Î∞úÌòÑ ÏÝïÎèÑÏóê ÌܵÍ≥ÑÏÝÅ ÏúÝÏùòÏѱÏùÄ Î≥¥Í≥ÝÎêòÏßÄ ÏïäÏïòÎã§[1,2,6,7]. 91ΙÖÏùò ÌôòÏûêÏóêÏÑú ÏàòÏàÝ ÏÝÑ ÏòÅÏÉÅÌïôÏÝÅ Í≤ÄÏǨ Í≤∞Í≥ºÏôÄ ÏõêÎ∞ú Î∂ÄÏúÑ Îì± ÏûÑÏÉÅÏñëÏÉÅÏùÑ Í≥ÝÎݧÌïòÏó¨ Í≤ΩÎ∂ÄÏÝàÏÝúÏàÝ Ïó¨Î∂ÄΕº Í≤∞ÏÝïÌïòÏòÄÍ≥Ý, Í∑∏ Í≤∞Í≥º 42ΙÖÏùò N(+)Îäî ÏÑÝÌÉùÏÝÅ ÎòêÎäî ÏπòΣåÏÝÅ Í≤ΩÎ∂ÄÏÝàÏÝúÏàÝ ÏãúÌñâ ÌõÑ Ï°∞ÏßÅÍ≤ÄÏǨΰú ζºÌîÑÏÝà ÏÝÑÏù¥Í∞Ä ÌôïÏù∏Îêú ÌôòÏûêÏù¥Î©∞, 49ΙÖÏùò N(-)Îäî ÏÑÝÌÉùÏÝÅ Í≤ΩÎ∂ÄÏÝàÏÝúÏàÝ ÏãúÌñâ ÌõÑ Ï°∞ÏßÅÍ≤ÄÏǨÏóêÏÑú ζºÌîÑÏÝà ÏÝÑÏù¥Í∞Ä Í¥ÄÏ∞∞ÎêòÏßÄ ÏïäÏùÄ ÌôòÏûê 22ΙÖÍ≥º ÏòÅÏÉÅ ÏßÑÎã®ÏóêÏÑú Í≤ΩÎ∂Ä ÏÝÑÏù¥Í∞Ä ÏùòÏã¨ÎêòÏßÄ ÏïäÏúºÎ©∞ ÏûÝÏû¨ ÏÝÑÏù¥ Í∞ÄÎä•ÏѱÏù¥ ÎÇÆÏïÑ Í≤ΩÎ∂ÄÏÝàÏÝúÏàÝÏùÑ ÏãúÌñâÌïòÏßÄ ÏïäÏùÄ 27ΙÖÏúºÎ°ú ͵¨ÏѱÎêòÏñ¥ ÏûàÎã§. Í≤ΩÎ∂ÄÏÝàÏÝúÏàÝÏùÑ ÏãúÌñâÌïòÏßÄ ÏïäÏùÄ 27ΙÖÏùò ÌôòÏûêÎäî Ï£ºÎ°ú Í≤ΩÎ∂Ä ÏÝÑÏù¥Í∞Ä ÎìúΨ∏ ÌõÑÎëêÏïîÏù¥ÎÇò Í∑∏ Ïô∏ TÎ≥ëÍ∏∞Í∞Ä ÎÇÆÏùÄ Ï°∞Í∏∞Ïùò ͵¨Í∞ïÏïî ÌôòÏûêÎì§Ïù¥ÏóàÍ≥Ý, Ï∂îÏÝŠͥÄÏ∞∞ÏóêÏÑú Í≤ΩÎ∂Ä ÏÝÑÏù¥Í∞Ä Î∞úÍ≤¨Îêú Í≤ΩÏö∞Îäî ÏóÜÏóàÎã§.
Î≥∏ Ïó∞͵¨Ïùò ÌïúÍ≥ÑÏÝêÏúºÎ°úÎäî Ï≤´Ïß∏, ÌõÑÌñ•ÏÝÅÏúºÎ°ú ÏßÑÌñâÎêú Ïó∞͵¨ÎùºÎäî ÏÝê, Îëê Î≤àÏß∏ΰúÎäî ÏõêÎ∞ú Î∂ÄÏúÑÎ≥Ñ ÌëúÎ≥∏ ÏàòÍ∞Ä Í≥ÝΕ¥ÏßÄ Î™ªÌïú ÏÝêÏù¥Î©∞, ÏÑ∏ Î≤àÏß∏ΰúÎäî Ï¢ÖÏñë Ï°∞ÏßÅÍ≥º ÎèôÏùºÌïú ÌôòÏûêÏóêÏÑúÏùò ÏÝïÏÉÅ Ï°∞ÏßÅÍ≥ºÏùò ÎπÑ͵êÍ∞Ä Ïù¥Î£®Ïñ¥ÏßÄÏßÄ Î™ªÌïú ÏÝêÏù¥Îã§. Î≥∏ Ïó∞͵¨Îäî ÎëêÍ≤ΩÎ∂Ä Ìé∏ÌèâÏÑ∏Ìè¨ÏïîÏóêÏÑú CLDN-1Ïùò Í∞ïÌïú Î∞úÌòÑÏù¥ Ï¢ÖÏñëÏùò ζºÌîÑ관 Ïπ®Ïú§ÏѱÏùÑ Ï¶ùÍ∞ÄÏãúÌǧΩ∞ ÎÇÆÏùÄ ÏÉùÏ°¥Ïú®Í≥º ÏúÝÏùòÌïú Í¥ÄÎÝ®ÏùÑ Î≥¥Ïù∏Îã§Îäî Í≤∞Í≥ºÎ•º ÏñªÏóàÎã§. Í∑∏Îü¨ÎÇò ÏõêÎ∞ú Î∂ÄÏúÑÎ≥Ñΰú ͵¨Í∞ïÏïîÎßåÏùÑ ÎåÄÏÉÅÏúºÎ°ú ÌñàÏùÑ Îïê Ïù¥ÏÝÑ Íµ¨Í∞ïÏïîÏóêÏÑú CLDN-1 Î∞úÌòÑÍ≥º Í¥ÄÎÝ®ÌïòÏó¨ Î≥¥Í≥ÝÎêú ΙáΙá Ïó∞͵¨ÏôÄÎäî Îã§Î•∏ Í≤∞Í≥ºÎ•º Î≥¥ÏòÄÎã§. Dos Reis Îì±[7]Ïùò Ïó∞͵¨ÏóêÏÑúÎäî ͵¨Í∞ïÏïîÏóêÏÑú Î∞úÌòÑÏù¥ ϶ùÍ∞ÄÎêú CLDN-1Ïù¥ Í≥µÍ≤©ÏÝÅÏù∏ ÏïîÏùò ÌäπÏѱÏóêÏÑú Î≥¥Ïù¥Îäî ÌòàÍ¥ÄζºÌîÑ관 Ïπ®ÏäµÍ≥º ÏãÝÍ≤ΩÏ£ºÏúÑ Ïπ®ÏäµÍ≥º Ïó∞Í¥ÄÏѱÏù¥ ÏûàÎã§Í≥Ý Î≥¥Í≥ÝÌïòÏòÄÎã§. ÎòêÌïú SappayatosokÍ≥º Phattarataratip [2]Ïùò Ïó∞͵¨ÏóêÏÑúÎäî ͵¨Í∞ïÏïîÏóêÏÑú CLDN-1Ïùò ϶ùÍ∞ÄÎêú Î∞úÌòÑÏù¥ ÏûÑÏÉÅ Î≥ëÍ∏∞ÏôÄ ÏïîÏùò Î≥ëζ¨ÌïôÏÝÅ ÌäπÏѱ ϧë ÏãÝÍ≤ΩÏ£ºÏúÑ Ïπ®Ïäµ, Ìòà관 Ïπ®Ïäµ, ζºÌîÑÏÝà ÏÝÑÏù¥ÏôÄ Ïó∞Í¥ÄÎêúÎã§Í≥Ý Î∞ùÌòîÎã§. Î≥∏ Ïó∞͵¨ÏóêÏÑúÎäî ÏÝÑÏ≤¥ ÎëêÍ≤ΩÎ∂ÄÏïîÏóêÏÑúÎäî CLDN-1 Í∞ïÏñëÏѱ Î∞úÌòÑ͵∞ÏóêÏÑú ζºÌîÑ관 Ïπ®Ïú§Ïù¥ ϶ùÍ∞ÄÌïúÎã§Îäî Í≤∞Í≥ºÎ•º ÏñªÏóàÏúºÎÇò ͵¨Í∞ïÏïî 23ÏòàÎßåÏùÑ ÎåÄÏÉÅÏúºÎ°ú ÌñàÏùÑ ÎïåÏóî ÌܵÍ≥ÑÏÝÅ ÏúÝÏùòÏѱÏùÑ ÏñªÏßÄ Î™ªÌñàÎã§. Ïù¥Îü¨Ìïú Í≤∞Í≥ºÏùò Ï∞®Ïù¥Îäî Î≥∏ Ïó∞͵¨Ïùò ͵¨Í∞ïÏïîÏóêÏÑú Ï¢ÖÏñëÏùò Ïπ®ÏäµÏù¥ Í¥ÄÏ∞∞Îêú ÌëúÎ≥∏ ÏàòÍ∞Ä ÏúÑ Ïó∞͵¨ÏóêÏÑú Î≥¥Í≥ÝÎêú ͱ¥ÏàòÏóê ÎπÑÌï¥ ÏÝÅÏùÄ Í≤ÉÏóêÏÑú Í∏∞Ïù∏ÌñàÏùÑ Í≤ÉÏù¥Îùº ÏǨΣåÎêúÎã§. Î≥∏ Ïó∞͵¨ÏóêÏÑúÎäî ͵¨Í∞ïÏïî 23Ïòà ϧë ζºÌîÑ관 Ïπ®Ïú§Ïù¥ 2Ïòà(8.7%)ÏóêÏÑúÎßå Í¥ÄÏ∞∞ÎêòΩ∞, Ìòà관 Ïπ®Ïú§ÏùÄ 1Ïòà(4.3%), ÏãÝÍ≤ΩÏ£ºÏúÑ Ïπ®ÏäµÏùÄ 4Ïòà(17.4)Í∞Ä Í¥ÄÏ∞∞ÎêòÏóàÍ≥Ý, SappayatosokÍ≥º Phattarataratip [2]Ïùò Ïó∞͵¨ÏóêÏÑúÎäî ͵¨Í∞ïÏïî ÌôòÏûê 45ÏòàΕº ÎåÄÏÉÅÏúºÎ°ú Ìòà관 Ïπ®Ïäµ 19Ïòà(42.2), ÏãÝÍ≤ΩÏ£ºÏúÑ Ïπ®Ïäµ 17Ïòà(37.8%)Í∞Ä Í¥ÄÏ∞∞ÎêòÏóàÎã§. ClaudinÏùÄ Î∞ÄÏ∞©Ïó∞ÏÝëÏùò Í∏∞Îä•ÏùÑ ÏúÝÏßÄÌïòÎäî Îç∞ ϧëÏöîÌïú Ïó≠ÌïÝÏùÑ ÌïòÍ≥Ý ÏûàÏúºÎ©∞, ÎëêÍ≤ΩÎ∂Ä Ìé∏ÌèâÏÑ∏Ìè¨ÏïîÏóêÏÑú ÎπÑÏÝïÏÉÅÏÝÅÏúºÎ°ú Î∞úÌòÑÏù¥ ϶ùÍ∞ÄÎêú CLDN-1Ïù¥ Î∞ÄÏ∞©Ïó∞ÏÝëÏùò ÏÝïÏÉÅÏÝÅÏù∏ ͵¨Ï°∞ÏôÄ Í∏∞Îä•ÏùÑ Î≥ÄÌôîÏãúÌÇ¥ÏúºÎ°úÏç® Ï¢ÖÏñëÏùò ζºÌîÑ관 Ïπ®Ïú§, Ï¢ÖÏñëÏùò Ïπ®ÏäµÏѱÏùÑ Ï¶ùÍ∞ÄÏãúÌǧÎäî Îç∞ ÏòÅÌñ•ÏùÑ Ï§Ñ Í≤ÉÏúºÎ°ú Î≥¥Ïó¨ÏßÑÎã§[20]. ÏùºÎ∂Ä Í≥ÝÌòï Ï¢ÖÏñëÏóêÏÑúÎäî Ï¢ÖÏñëÏùò ζºÌîÑ관 Ïπ®Ïú§Ïù¥ ÏòàÌõÑÏóê ÎØ∏ÏπòÎäî ϧëÏöîÏѱÏù¥ Ïûò ÏïåÎݧÏÝ∏ ÏûàÎäî Í≤ÉÏóê Î∞òÌï¥[25-27], ÎëêÍ≤ΩÎ∂Ä Ìé∏Ìèâ ÏÑ∏Ìè¨ÏïîÏóêÏÑúÎäî ÎßéÏùÄ Ïó∞͵¨Í∞Ä Î≥¥Í≥ÝÎêòÏóàÏúºÎÇò ÏïÑÏßÅÍπåÏßÄÎäî Ïù¥Ïóê ÎåÄÌïú Ï∂©Î∂ÑÌïú Ìï©ÏùòÍ∞Ä Ïù¥Î£®Ïñ¥ÏßÄÏßÄ ÏïäÏïòÎã§[28-30]. Jones Îì±[31]ÏùÄ Íµ¨Í∞ïÏïîÏóêÏÑú ζºÌîÑ관 Ïπ®Ïú§Ïù¥ ÏÉùÏ°¥Ïú®Ïóê ÏòÅÌñ•ÏùÑ ÎØ∏ÏπúÎã§Í≥Ý Î≥¥Í≥ÝÌïòÏòÄÍ≥Ý, ÎòêÌïú ζºÌîÑ관 Ïπ®Ïú§Í≥º Í≤ΩÎ∂Ä Î¶ºÌîÑÏÝà ÏÝÑÏù¥ÏôÄÏùò Ïó∞Í¥ÄÏѱÏóê ÎåÄÌï¥ÏÑúÎèÑ Î≥¥Í≥ÝÌïòÏòÄÎã§. Ïù¥Îü¨Ìïú Ïó∞͵¨ Í≤∞Í≥ºÎäî Îã§Î•∏ ÎπÑÏä∑Ìïú Ïó∞͵¨Îì§ÏóêÏÑú Ï∞æÏïÑÎ≥º Ïàò ÏûàÏóàÏúºÎÇò[32,33] Ι®ÎìÝ Ïó∞͵¨ÏóêÏÑú ζºÌîÑ관 Ïπ®Ïú§Í≥º Í≤ΩÎ∂Ä Î¶ºÌîÑÏÝà ÏÝÑÏù¥ÏôÄÏùò Ïó∞Í¥ÄÏѱÏùÑ ÏùºÍ¥ÄÎêòÍ≤å ÏûÖ϶ùÌïòÏßÄÎäî ΙªÌñàÎã§. Ìñ•ÌõÑ ÎëêÍ≤ΩÎ∂ÄÏïîÏùò Î∂ÑÏûêÏÝÅ Í∏∞ÏÝÑÍ≥º CLDN-1Ïóê ÎåÄÌïú Ï∂îÍ∞ÄÏÝÅÏù∏ Ïó∞͵¨Î•º ÌܵÌï¥ CLDN-1ÏùÄ ÎëêÍ≤ΩÎ∂ÄÏïîÏóêÏÑú ÏúÝÏö©Ìïú ÏòàÌõÑ Ïù∏Ïûêΰú Ïì∞Ïùº Ïàò ÏûàÏùÑ Í≤ÉÏù¥Î©∞, Îçî ÎÇòÏïÑÍ∞Ä Î∂ÑÏûêÏÝÅ ÏπòΣå ÏòÅÏó≠ÏóêÏÑú ÌëúÏÝÅ ÏπòΣåÏóêÎèÑ Ïù¥Ïö©ÎêÝ Ïàò ÏûàÏùÑ Í≤ÉÏúºÎ°ú Í∏∞ÎåÄÎêúÎã§.
ACKNOWLEDGMENTSThis study was supported by a National Research Foundation of Korea (NRF) grant funded by the Korean government (NRF-2020R1F1A1071489 to SH Lee)
NotesAuthor Contribution Conceptualization: Sang Hyuk Lee, Sung Im Do. Data curation: Jin Lee, Sung Im Do, Hyun Joo Lee. Investigation: Sun Woo Kim, Sung Min Jin. Methodology: Jin Lee, Sung Im Do, Hyun Joo Lee. Project administration: Jin Lee. Software: Jin Lee. Supervision: Sang Hyuk Lee, Sung Im Do, Hyun Joo Lee. Validation: Jin Lee, Sung Min Jin. Visualization: Jin Lee, Sun Woo Kim. Writing‚Äîoriginal draft: Jin Lee. Writing‚Äîreview & editing: Sang Hyuk Lee, Jin Lee. Fig.¬Ý1.Representative photomicrographs of immunohistochemical staining for CLDN-1 in HNSCC (magnification √ó200, √ó400). CLDN-1 staining was read as meaningful when it showed a clear brown reaction to the cell membrane. CLDN-1 staining intensity was scored on a scale of 0 to 3. 0: negative CLDN-1 expression (A), 1: weak CLDN-1 expression (B), 2: moderate CLDN-1 expression (C), 3: strong CLDN-1 expression (D). CLDN-1: claudin-1. 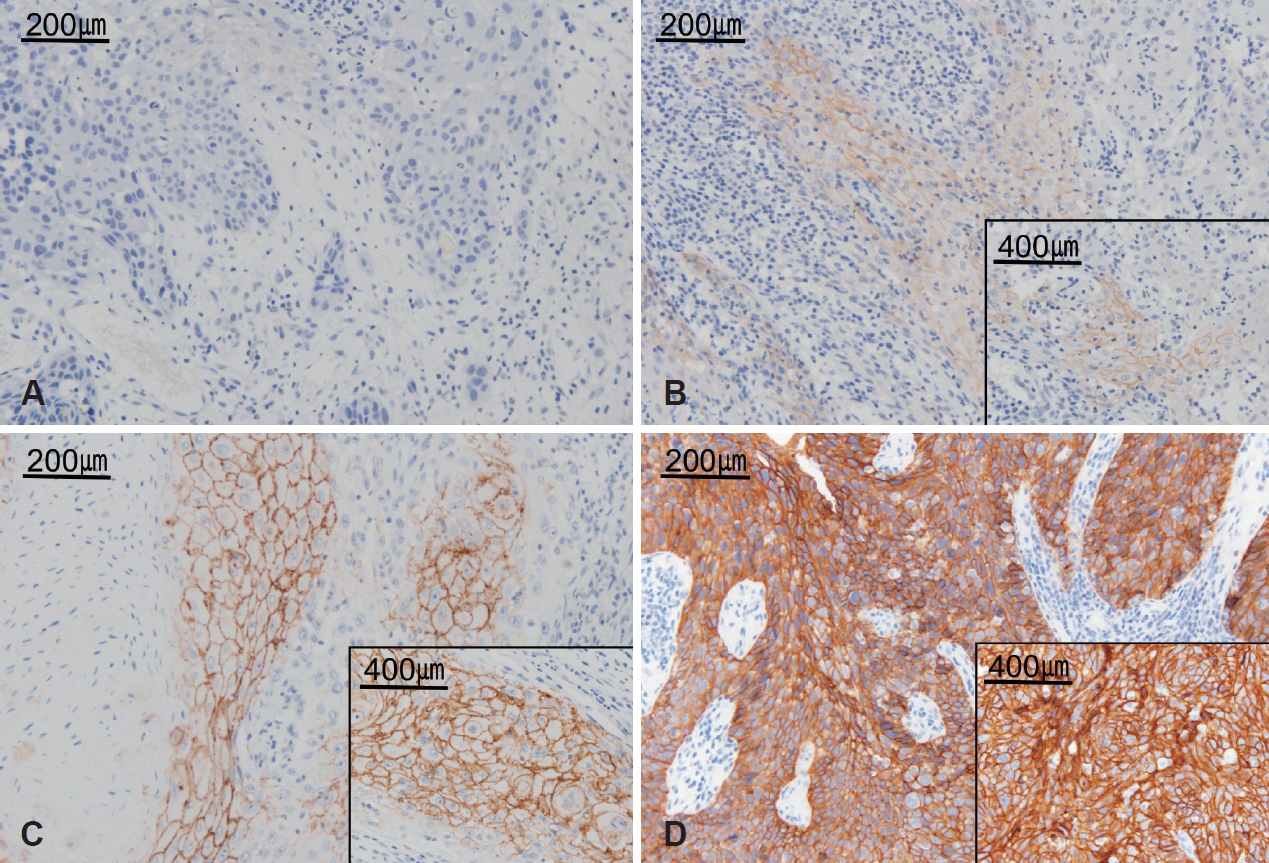
Fig.¬Ý2.Kaplan-Meier OS curve of head and neck squamous cell carcinoma patients with low versus high expression of claudin-1 (p=0.022). OS: overall survival. 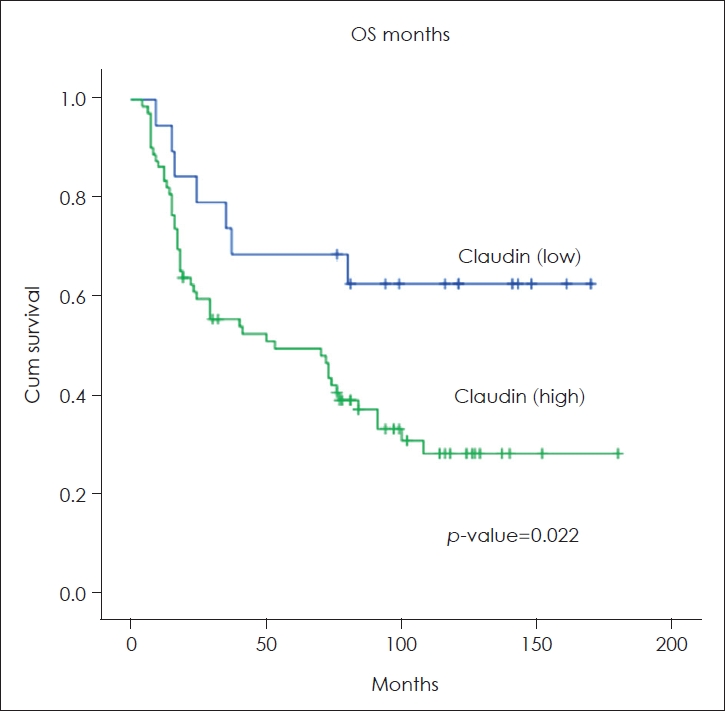
Table¬Ý1.Relationship between CLDN-1 expression and clinicopathological parameters for patients with head and neck squamous cell carcinoma Table¬Ý2.Analysis of relationship between CLDN-1 expression and lymphatic invasion according to primary site
Table¬Ý3.Multivariate analysis of variables predicting lymph node metastasis
REFERENCES1. Nelhűbel GA, Károly B, Szabó B, Lotz G, Kiss A, Tóvári J, et al. The prognostic role of claudins in head and neck squamous cell carcinomas. Pathol Oncol Res 2014;20(1):99-106.
2. Sappayatosok K, Phattarataratip E. Overexpression of claudin-1 is associated with advanced clinical stage and invasive pathologic characteristics of oral squamous cell carcinoma. Head Neck Pathol 2015;9(2):173-80.
3. Sobel G, Páska C, Szabó I, Kiss A, Kádár A, Schaff Z. Increased expression of claudins in cervical squamous intraepithelial neoplasia and invasive carcinoma. Hum Pathol 2005;36(2):162-9.
4. Kondoh A, Takano K, Kojima T, Ohkuni T, Kamekura R, Ogasawara N, et al. Altered expression of claudin-1, claudin-7, and tricellulin regardless of human papilloma virus infection in human tonsillar squamous cell carcinoma. Acta Otolaryngol 2011;131(8):861-8.
5. Escudero-Esparza A, Jiang WG, Martin TA. The claudin family and its role in cancer and metastasis. Front Biosci (Landmark Ed) 2011;16:1069-83.
6. Lourenço SV, Coutinho-Camillo CM, Buim ME, Pereira CM, Carvalho AL, Kowalski LP, et al. Oral squamous cell carcinoma: Status of tight junction claudins in the different histopathological patterns and relationship with clinical parameters. A tissue-microarray-based study of 136 cases. J Clin Pathol 2010;63(7):609-14.
7. Dos Reis PP, Bharadwaj RR, Machado J, Macmillan C, Pintilie M, Sukhai MA, et al. Claudin 1 overexpression increases invasion and is associated with aggressive histological features in oral squamous cell carcinoma. Cancer 2008;113(11):3169-80.
8. Schneeberger EE, Lynch RD. The tight junction: A multifunctional complex. Am J Physiol Cell Physiol 2004;286(6):C1213-28.
9. Tsukita S, Furuse M, Itoh M. Multifunctional strands in tight junctions. Nat Rev Mol Cell Biol 2001;2(4):285-93.
10. Mina LA, Sledge GW Jr. Rethinking the metastatic cascade as a therapeutic target. Nat Rev Clin Oncol 2011;8(6):325-32.
11. Li WJ, Zhang ZL, Yu XM, Cai XL, Pan XL, Yang XY. Expression of claudin-1 and its relationship with lymphatic microvessel generation in hypopharyngeal squamous cell carcinoma. Genet Mol Res 2015;14(4):11814-26.
13. Weinstein RS, Merk FB, Alroy J. The structure and function of intercellular junctions in cancer. Adv Cancer Res 1976;23:23-89.
14. Soler AP, Miller RD, Laughlin KV, Carp NZ, Klurfeld DM, Mullin JM. Increased tight junctional permeability is associated with the development of colon cancer. Carcinogenesis 1999;20(8):1425-31.
15. Martin TA, Jiang WG. Tight junctions and their role in cancer metastasis. Histol Histopathol 2001;16(4):1183-95.
16. Wodarz A. Tumor suppressors: Linking cell polarity and growth control. Curr Biol 2000;10(17):R624-6.
17. Oku N, Sasabe E, Ueta E, Yamamoto T, Osaki T. Tight junction protein claudin-1 enhances the invasive activity of oral squamous cell carcinoma cells by promoting cleavage of laminin-5 gamma2 chain via matrix metalloproteinase (MMP)-2 and membrane-type MMP-1. Cancer Res 2006;66(10):5251-7.
18. Morin PJ. Claudin proteins in human cancer: Promising new targets for diagnosis and therapy. Cancer Res 2005;65(21):9603-6.
19. Heiskala M, Peterson PA, Yang Y. The roles of claudin superfamily proteins in paracellular transport. Traffic 2001;2(2):92-8.
20. Harhaj NS, Antonetti DA. Regulation of tight junctions and loss of barrier function in pathophysiology. Int J Biochem Cell Biol 2004;36(7):1206-37.
21. Mitic LL, Van Itallie CM, Anderson JM. Molecular physiology and pathophysiology of tight junctions I. Tight junction structure and function: Lessons from mutant animals and proteins. Am J Physiol Gastrointest Liver Physiol 2000;279(2):G250-4.
22. Ding L, Lu Z, Lu Q, Chen YH. The claudin family of proteins in human malignancy: A clinical perspective. Cancer Manag Res 2013;5:367-75.
23. Morohashi S, Kusumi T, Sato F, Odagiri H, Chiba H, Yoshihara S, et al. Decreased expression of claudin-1 correlates with recurrence status in breast cancer. Int J Mol Med 2007;20(2):139-43.
24. Myal Y, Leygue E, Blanchard AA. Claudin 1 in breast tumorigenesis: Revelation of a possible novel “claudin high” subset of breast cancers. J Biomed Biotechnol 2010;2010:956897.
25. Algaba F. Lymphovascular invasion as a prognostic tool for advanced bladder cancer. Curr Opin Urol 2006;16(5):367-71.
26. Kim JM, Kim TY, Kim WB, Gong G, Kim SC, Hong SJ, et al. Lymphovascular invasion is associated with lateral cervical lymph node metastasis in papillary thyroid carcinoma. Laryngoscope 2006;116(11):2081-5.
27. Woo CS, Silberman H, Nakamura SK, Ye W, Sposto R, Colburn W, et al. Lymph node status combined with lymphovascular invasion creates a more powerful tool for predicting outcome in patients with invasive breast cancer. Am J Surg 2002;184(4):337-40.
28. Fives C, Feeley L, O’Leary G, Sheahan P. Importance of lymphovascular invasion and invasive front on survival in floor of mouth cancer. Head Neck 2016;38 Suppl 1:E1528-34.
29. Adel M, Kao HK, Hsu CL, Huang JJ, Lee LY, Huang Y, et al. Evaluation of lymphatic and vascular invasion in relation to clinicopathological factors and treatment outcome in oral cavity squamous cell carcinoma. Medicine (Baltimore) 2015;94(43):e1510.
30. Jardim JF, Francisco AL, Gondak R, Damascena A, Kowalski LP. Prognostic impact of perineural invasion and lymphovascular invasion in advanced stage oral squamous cell carcinoma. Int J Oral Maxillofac Surg 2015;44(1):23-8.
31. Jones HB, Sykes A, Bayman N, Sloan P, Swindell R, Patel M, et al. The impact of lymphovascular invasion on survival in oral carcinoma. Oral Oncol 2009;45(1):10-5.
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 |
 |